金賽藥業金納單抗注射液臨床試驗申請獲批
發布時間
2024-05-23
閱讀量
1901
分(fēn)享
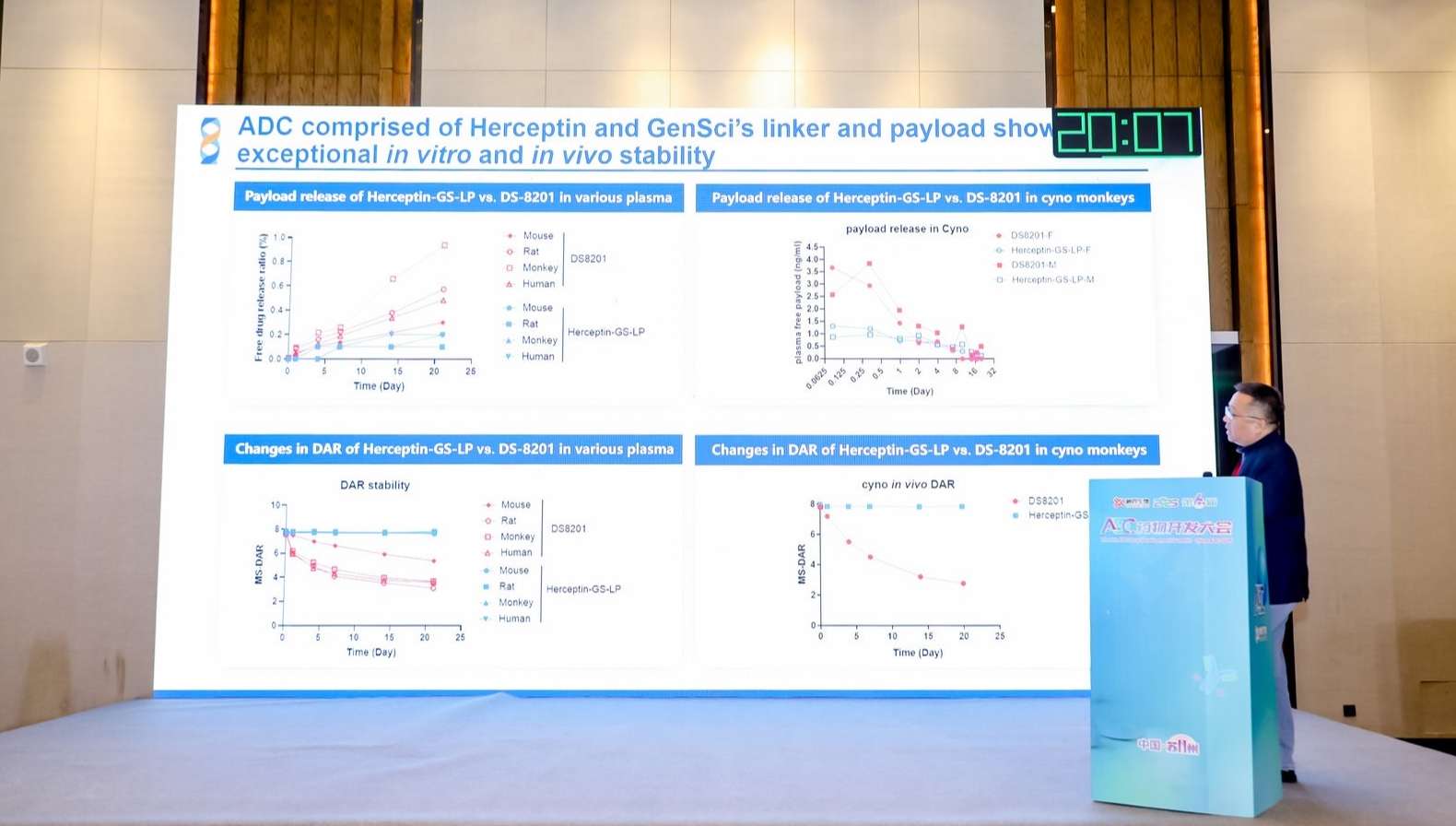
近日,金賽藥業收到國(guó)家藥品監督管理(lǐ)局(NMPA)關于金納單抗注射液的《藥物(wù)臨床試驗批準通知書》,以開展金納單抗注射液新(xīn)劑型的生物(wù)等效性研究。
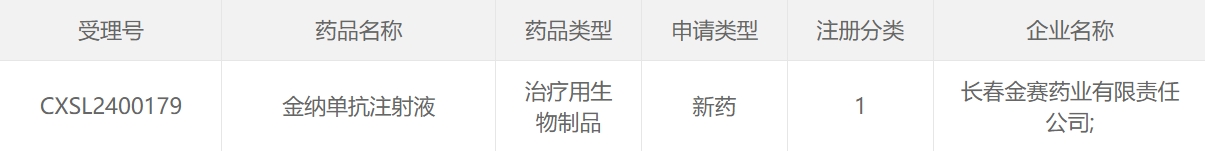 截圖源自:CDE官網
截圖源自:CDE官網
金賽藥業旗下金納單抗是一款治療用(yòng)生物(wù)制品 1 類新(xīn)藥,是通過基因工(gōng)程技(jì )術等進行生産(chǎn)的抗 IL-1β抗體(tǐ)藥物(wù)。此前,注射用(yòng)金納單抗(抗IL-1β抗體(tǐ))急性痛風性關節炎适應症的上市申請已經獲得國(guó)家藥監局受理(lǐ);全身型幼年特發性關節炎、間質(zhì)性肺病等适應症正處于臨床研究階段。此次獲批的臨床試驗系金納單抗注射液這一新(xīn)劑型的生物(wù)等效性研究。
相關研究表明,過量的白介素是多(duō)種炎症疾病的緻病因素,抗白介素-1β(IL-1β)抗體(tǐ)可(kě)以快速和特異性地阻斷IL-1β與其受體(tǐ)的結合,從而阻斷炎症發生。