2024 ACR | 中(zhōng)國(guó)首款IL-1β單克隆抗體(tǐ)治療急性痛風性關節炎數據亮眼
發布時間
2024-11-18
閱讀量
3349
分(fēn)享
美國(guó)風濕病學(xué)會(ACR)學(xué)術年會是風濕病學(xué)領域備受關注的年度盛會,2024 ACR年會于11月14日-19日在美國(guó)華盛頓特區(qū)隆重召開,會議展示了風濕病學(xué)最新(xīn)的前沿進展及研究成果!本次大會上,國(guó)産(chǎn)1.1類新(xīn)藥IL-1β單克隆抗體(tǐ)伏欣奇拜單抗(Firsekibart)[曾用(yòng)名(míng):金納單抗(Genakumab)]在大會上公(gōng)布了最新(xīn)的治療急性痛風性關節炎的III期臨床研究結果,備受全球學(xué)術界矚目。

FDA已批準IL-1β單克隆抗體(tǐ)用(yòng)于治療急性痛風性關節炎
有(yǒu)“王者之病”之稱的痛風曾被視為(wèi)一種富貴病,但随着經濟發展和生活水平的不斷提高,痛風已然成為(wèi)成人中(zhōng)常見的一種炎症性關節炎。高尿酸血症是痛風發生的病理(lǐ)基礎,近年來,高尿酸血症的患病率不斷升高,也被稱為(wèi)“第四高”。中(zhōng)華醫(yī)學(xué)會内分(fēn)泌學(xué)分(fēn)會全國(guó)31省市流行病學(xué)TIDE研究顯示,成人高尿酸血症總體(tǐ)标化患病率高達17.7%,2015-2017年間約有(yǒu)1.85億人患有(yǒu)高尿酸血症,而痛風的總體(tǐ)标化患病率也達到了3.2%,估計在2015-2017年間中(zhōng)國(guó)成人痛風患者有(yǒu)2556萬[1]。
大部分(fēn)痛風患者使用(yòng)降尿酸藥物(wù),以及急性發作(zuò)時使用(yòng)非甾體(tǐ)類抗炎藥(NSAIDs)、秋水仙堿及糖皮質(zhì)激素等藥物(wù)可(kě)有(yǒu)效控制病情。但有(yǒu)部分(fēn)痛風患者,病程時間長(cháng),血尿酸控制水平難以達标,急性痛風性關節炎反複發作(zuò),應用(yòng)上述一線(xiàn)治療藥物(wù)不佳或存在用(yòng)藥禁忌症的急性痛風性關節炎患者,目前國(guó)内外指南均推薦使用(yòng)IL-1抑制劑進行治療,且美國(guó)食品藥品監督管理(lǐ)局(FDA)在2023年8月也正式批準了IL-1β單克隆抗體(tǐ)——卡那單抗用(yòng)于治療這類型的痛風患者的急性發作(zuò)[2] 。
ILARIS(卡那單抗),用(yòng)于非甾體(tǐ)抗炎藥(NSAID)和秋水仙堿禁忌症、不能(néng)耐受或不能(néng)提供足夠的應答(dá)以及不适合重複使用(yòng)皮質(zhì)類固醇的成年痛風發作(zuò)患者的對症治療。
伏欣奇拜單抗或可(kě)成為(wèi)IL-1β抑制劑類“Best-in-class”
截至目前,我國(guó)尚未有(yǒu)白介素-1β(IL-1β)的單克隆抗體(tǐ)藥物(wù)上市,急性痛風性關節炎反複發作(zuò)患者的臨床治療需求亟待滿足。今年4月,國(guó)内自主研發的1.1類新(xīn)藥IL-1β單克隆抗體(tǐ)——伏欣奇拜單抗的上市申請已獲得國(guó)家藥品監督管理(lǐ)局受理(lǐ),用(yòng)于治療這類型的痛風性關節炎患者的急性發作(zuò)。此次ACR會議上就公(gōng)布了由複旦大學(xué)附屬華山(shān)醫(yī)院風濕科(kē)鄒和建教授牽頭的III期臨床研究(GUARD-1)結果。
GUARD-1研究是一項随機、雙盲雙模拟、陽性對照的III期臨床試驗,對急性痛風性關節炎發作(zuò)的患者,對比使用(yòng)複方倍他(tā)米松治療和伏欣奇拜單抗治療的效果。該研究納入313名(míng)18~75歲符合ACR 2015痛風診斷标準的急性痛風性關節炎發作(zuò)的患者,患者對NSAIDs和/或秋水仙堿有(yǒu)禁忌症、不耐受或應答(dá)不佳,且在過去一年内痛風發作(zuò)≥2次,按1:1随機分(fēn)為(wèi)伏欣奇拜單抗治療組(n=157)和複方倍他(tā)米松治療組(n=156),分(fēn)别給與伏欣奇拜單抗200mg 皮下注射、複方倍他(tā)米松7mg 肌肉注射治療。研究治療周期為(wèi)48周,前24周為(wèi)雙盲治療期,24周後開放标簽(所有(yǒu)受試者均可(kě)接受伏欣奇拜單抗治療)。研究設計主要終點為(wèi)雙終點設計:評價兩組急性痛風性關節炎發作(zuò)患者的72小(xiǎo)時疼痛VAS評分(fēn)(非劣效檢驗)和12周内首次複發中(zhōng)位時間(優效檢驗)。
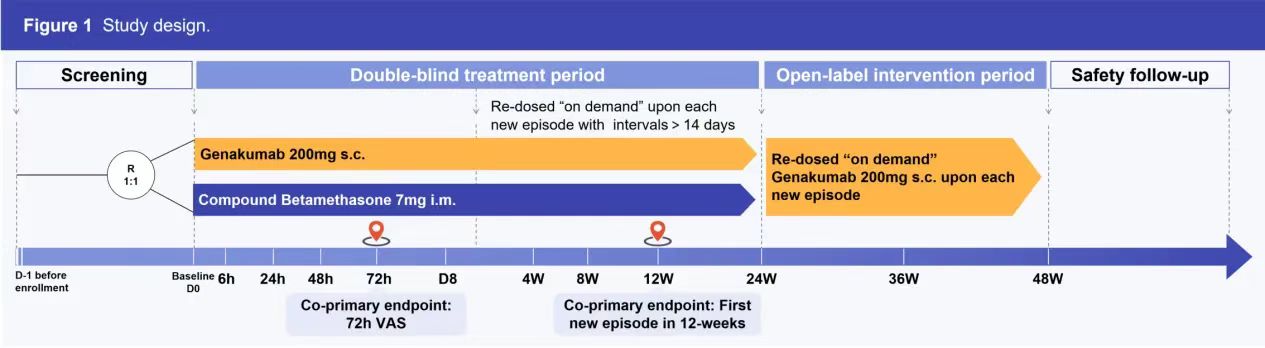
圖1.研究設計
最終研究入組的人群中(zhōng)位年齡42歲,98.7%的患者為(wèi)男性,患者的平均病程時長(cháng)為(wèi)約8.7年,大多(duō)數患者在前一年報告過 3 次以上痛風發作(zuò)。在全分(fēn)析集(FAS)分(fēn)析中(zhōng),伏欣奇拜單抗組在72小(xiǎo)時急性痛風性關節炎疼痛緩解的VAS評分(fēn)上非劣效于複方倍他(tā)米松,且在48小(xiǎo)時後伏欣奇拜單抗組疼痛VAS評分(fēn)下降程度比複方倍他(tā)米松組趨勢更明顯。
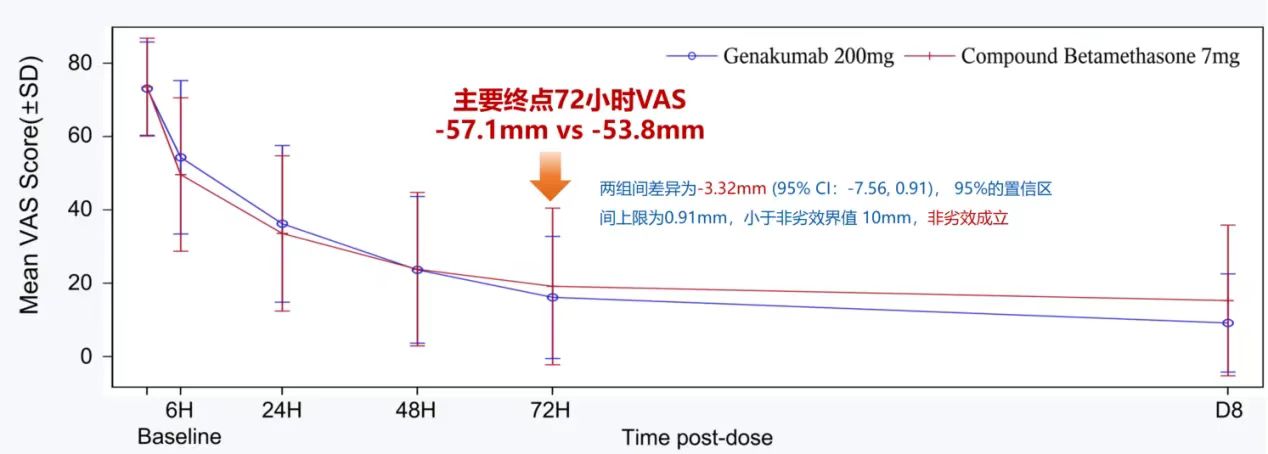
圖2.首次用(yòng)藥後8天内的平均疼痛強度VAS評分(fēn)的變化(0-100 mm)
在12周内首次複發中(zhōng)位時間上,伏欣奇拜單抗顯著延遲了患者的首次急性痛風性關節炎複發時間;對比複方倍他(tā)米松,伏欣奇拜單抗在12周時顯著降低了患者90%的首次急性痛風性關節炎複發風險(HR 0.10;95% CI:0.060, 0.169;p<0.0001),24周時首次複發風險降低了87%(HR 0.13;95% CI: 0.084, 0.208;p<0.0001)。這一數據目前可(kě)能(néng)是同類藥物(wù)在這類型痛風患者急性發作(zuò)時的最佳療效,伏欣奇拜單抗或可(kě)成為(wèi)IL-1β單克隆抗體(tǐ)中(zhōng)的“Best-in-class”。
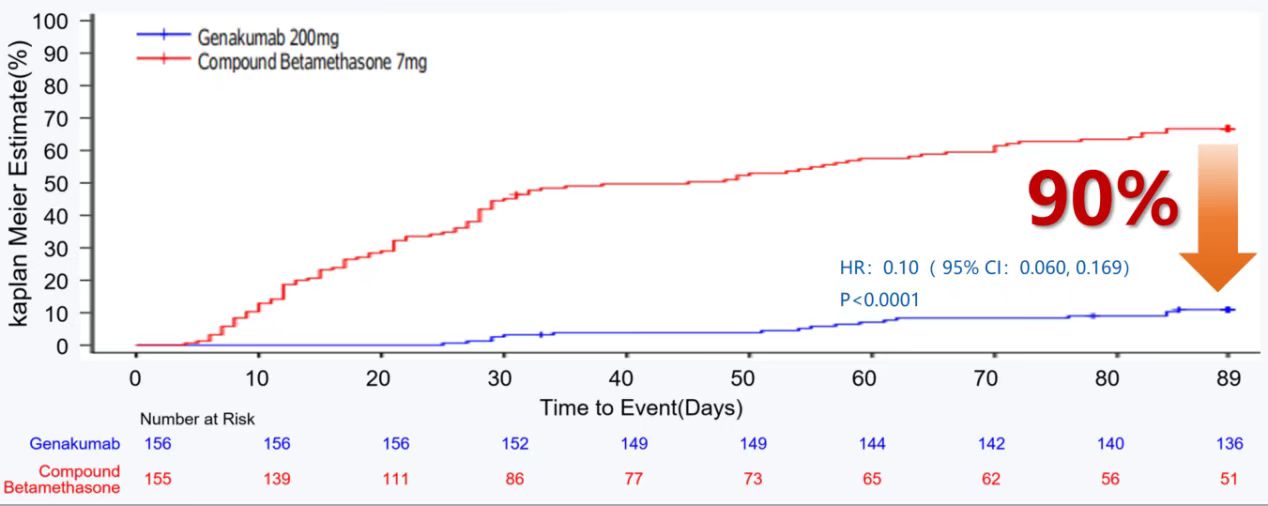
圖3.12周内首次新(xīn)發痛風事件時間(Kaplan-Meier 估計量)
在安(ān)全性方面,共計159例(51.0%)受試者出現治療相關不良事件,其中(zhōng)伏欣奇拜單抗組79例(50.6%),複方倍他(tā)米松組80例(51.3%)。複方倍他(tā)米松組共有(yǒu)3例患者報告了治療相關嚴重不良事件[3] 。
對NSAIDs和/或秋水仙堿禁忌、不耐受或缺乏療效的,以及不适合反複使用(yòng)類固醇激素的成年痛風性關節炎急性發作(zuò)的患者,伏欣奇拜單抗在痛風發作(zuò)急性期更安(ān)全,緩解急性痛風性關節炎發作(zuò)時的疼痛方面非劣于複方倍他(tā)米松;在緩解期能(néng)更有(yǒu)效的延緩痛風的急性複發,在用(yòng)藥12周及24周内可(kě)顯著降低患者痛風複發的風險(分(fēn)别降低90%和87%),顯著延長(cháng)患者痛風急性複發的時間。
這一組引人注目的臨床研究數據,激發了醫(yī)患群體(tǐ)對于國(guó)内自主研發的1.1類新(xīn)藥——IL-1β單克隆抗體(tǐ)伏欣奇拜單抗的熱切期盼。大家衷心希望該藥物(wù)能(néng)夠加速推進上市進程,從而迅速填補國(guó)内在這一藥物(wù)類别上的空白,并為(wèi)飽受痛風性關節炎反複發作(zuò)之苦的患者帶來福音,讓他(tā)們能(néng)夠盡早擺脫病痛困擾!
參考文(wén)獻:
[1] Song J, Jin C, Shan Z, Teng W, Li J. Prevalence and Risk Factors of Hyperuricemia and Gout. J Transl Int Med. 2022;10(2):134-145. Published 2022 Jul 7. doi:10.2478/jtim-2022-0031
[2] https://www.medscape.com/viewarticle/995993
[3] Xue Y, Chu T, Hu J, Gou W, Zhang N, Li J, Yu J, Li S, Li S, Qian L, Duan X, Duan L, Zou H. Efficacy and Safety of Genakumab versus Compound Betamethasone in Gout: The GUARD-1 Study [abstract]. Arthritis Rheumatol. 2024; 76 (suppl 9). https://acrabstracts.org/abstract/efficacy-and-safety-of-genakumab-versus-compound-betamethasone-in-gout-the-guard-1-study/. Accessed November 13, 2024.