金賽藥業攜最新(xīn)研發成果出席JPM大會
發布時間
2025-01-21
閱讀量
1150
分(fēn)享
1月14日,金賽藥業研發及商(shāng)業化團隊相關代表出席全球醫(yī)療健康領域盛會——第43屆摩根大通醫(yī)療健康年會(J.P. Morgan Healthcare Conference,簡稱“JPM大會”),并帶來多(duō)領域研發管線(xiàn)成果分(fēn)享。
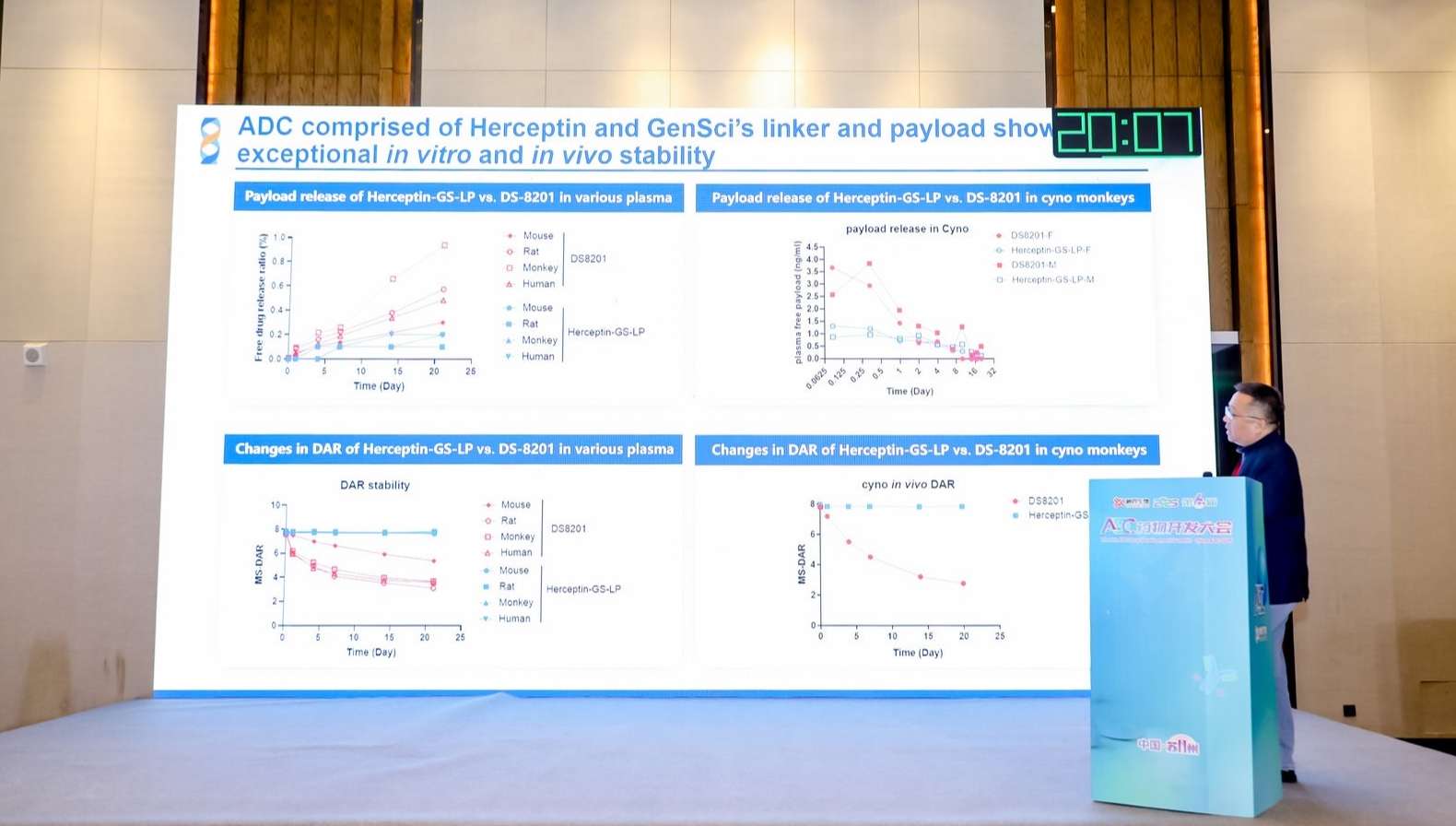
本次大會,金賽藥業分(fēn)享了覆蓋腫瘤、免疫、内分(fēn)泌、代謝(xiè)等多(duō)個重點疾病領域以及多(duō)個罕見病細分(fēn)領域的創新(xīn)研發管線(xiàn),涵蓋多(duō)個潛在First-in-Class(FIC)和Best-in-Class(BIC)創新(xīn)分(fēn)子。在腫瘤治療領域的産(chǎn)品組合中(zhōng),多(duō)款雙靶點ADC和小(xiǎo)分(fēn)子藥物(wù)在臨床前展現了Best-in-Class的巨大潛質(zhì)。
在免疫及呼吸領域,金賽藥業在大分(fēn)子和小(xiǎo)分(fēn)子進行了全方位的布局,其中(zhōng)NLRP3 抑制劑展現了明顯的臨床前Best-in-class潛質(zhì),尤其值得關注的是,金賽藥業也披露了一條吸入siRNA管線(xiàn),通過霧化給藥,吸入siRNA可(kě)進行基于mRNA的基因編輯來特異性地沉默疾病相關基因的表達,從而治療特發性肺纖維化等呼吸領域疾病。
在金賽持續深耕的代謝(xiè)内分(fēn)泌領域,金賽藥業自主研發的NK3R小(xiǎo)分(fēn)子拮抗劑GS1-144去年已獲美國(guó)食品藥品監督管理(lǐ)局(FDA)新(xīn)藥二期臨床試驗申請默示許可(kě),拟用(yòng)于治療絕經期血管舒縮症。早在2023年,GS1-144在同一适應症的臨床試驗申請已獲得中(zhōng)國(guó)國(guó)家藥品監督管理(lǐ)局批準。目前國(guó)内尚無NK3R靶點藥物(wù)上市,若GS1-144上市作(zuò)為(wèi)絕經期血管舒縮症的非激素口服療法,可(kě)以為(wèi)患者提供更好的治療選擇。
針對臨床未被滿足的罕見病診療需求,多(duō)年來金賽藥業持續投入創新(xīn)藥物(wù)開發,本次大會也帶來了針對囊性纖維化(CFTR mRNA)、苯丙酮尿症(小(xiǎo)分(fēn)子)和有(yǒu)機酸血症(PANK1/3激動劑)等罕見病的創新(xīn)管線(xiàn),以期為(wèi)全球罕見病患者提供更多(duō)的治療藥物(wù)選擇。
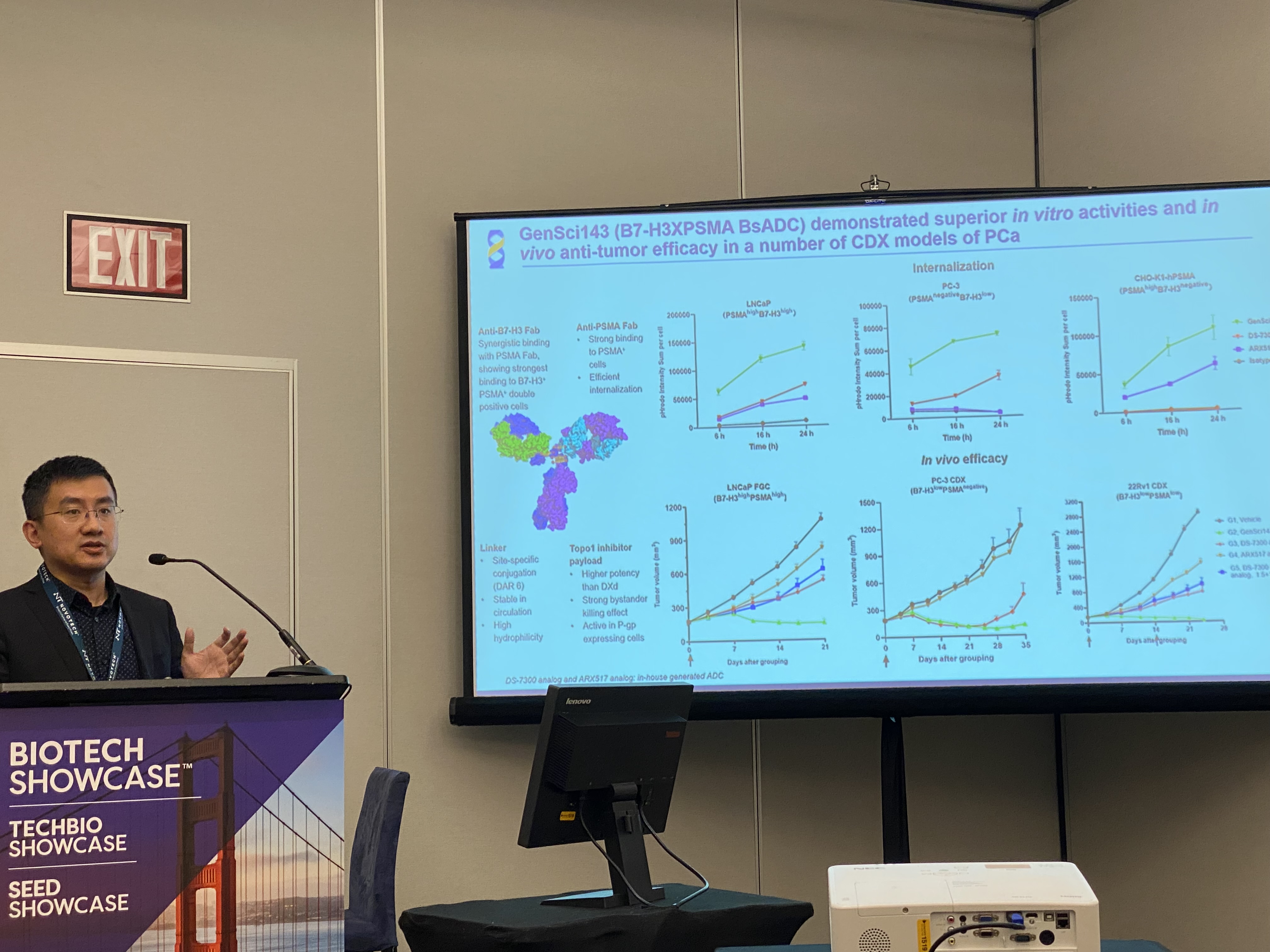
金賽藥業化藥生物(wù)學(xué)執行總監夏遠(yuǎn)峰與參會者交流
金賽藥業化藥生物(wù)學(xué)執行總監夏遠(yuǎn)峰表示,很(hěn)榮幸參加本屆大會,JPM大會作(zuò)為(wèi)全球生物(wù)醫(yī)藥健康領域規模最大、級别最高、最具(jù)信息量的産(chǎn)業交流合作(zuò)盛會之一,此次我們攜創新(xīn)研發管線(xiàn)亮相本次大會,希望與更多(duō)MNC及頭部醫(yī)藥企業達成戰略合作(zuò),共同推動創新(xīn)成果邁向國(guó)際市場,最終惠及全球患者。
金賽藥業全力構建全球醫(yī)藥創新(xīn)生态圈,高度重視産(chǎn)學(xué)研醫(yī)合作(zuò),通過院企合作(zuò)、授權合作(zuò)、股權投資、研發平台合作(zuò)等多(duō)樣化合作(zuò)方式,在藥物(wù)開發、臨床研究、生産(chǎn)和商(shāng)業化等多(duō)個環節、多(duō)個方面與合作(zuò)夥伴開展緊密合作(zuò)。目前公(gōng)司已合作(zuò)10餘家婦兒及綜合三甲醫(yī)院并有(yǒu)望拓展至20家,同時與全球10餘家頭部企業達成合作(zuò)。
促進源頭創新(xīn),為(wèi)公(gōng)司長(cháng)期高質(zhì)量發展提供源源不斷的動力。公(gōng)司構建的五大自主可(kě)控的技(jì )術平台,擁有(yǒu)生物(wù)藥、化學(xué)藥、特殊制劑、活菌藥、醫(yī)療器械及醫(yī)學(xué)營養品等創新(xīn)産(chǎn)品的全球研發與生産(chǎn)能(néng)力。創新(xīn)驅動發展,金賽藥業始終堅持對标國(guó)際最高研發标準,持續開拓差異化、高潛力、創新(xīn)性研發管線(xiàn)。
過去一年,金賽藥業研發成果進展亮眼:PD-1激動劑獲中(zhōng)國(guó)國(guó)家藥監局I類創新(xīn)藥臨床批件;針對甲狀腺相關眼病的促甲狀腺素受體(tǐ)(TSHR)的抗體(tǐ)分(fēn)子GenSci098和小(xiǎo)分(fēn)子KIF18A抑制劑GenSci122,已獲中(zhōng)國(guó)國(guó)家藥品監督管理(lǐ)局批準開展臨床試驗,并已獲得FDA臨床試驗默示許可(kě);國(guó)産(chǎn)1.1類新(xīn)藥IL-1β單克隆抗體(tǐ)伏欣奇拜單抗(Firsekibart)[曾用(yòng)名(míng):金納單抗(Genakumab)]最新(xīn)的治療急性痛風性關節炎的III期臨床研究結果顯示,伏欣奇拜單抗或可(kě)成為(wèi)IL-1β單克隆抗體(tǐ)中(zhōng)的“Best-in-class”。以上創新(xīn)成果的研發上市進展,有(yǒu)望持續勾畫金賽藥業未來的增長(cháng)曲線(xiàn)。